予路乾行的合作伙伴����,博瑞醫藥的雙GLP-1/GIP受體激動(dòng)劑BGM0504的分子設計策略和實(shí)驗結果于2024年7月19日在線(xiàn)發(fā)表于《Nature》子刊Scientific Reports���。博瑞醫藥(股票代碼:688166.SH)是一家參與國際競爭�����、專(zhuān)注于高端藥品研發(fā)的創(chuàng )新型制藥公司�����。文章工作由博瑞醫藥���、予路乾行以及武漢理工大學(xué)相關(guān)研究團隊合作完成�����。
發(fā)表在《Nature》子刊上的文章題為《利用分子動(dòng)力學(xué)優(yōu)化BGM0504�,增強雙靶點(diǎn)激動(dòng)作用�,以對抗糖尿病和肥胖癥(Molecular dynamics-guided optimization of BGM0504 enhances dual target agonism for combating diabetes and obesity)》��。本文由博瑞醫藥董事長(cháng)袁建棟博士和予路乾行計算部負責人劉文朗為共同第一作者���、博瑞醫藥和武漢理工大學(xué)作為共同通訊單位����。這一發(fā)現得到了多家海外知名媒體如美通社�、美聯(lián)社�、朝日新聞等機構的關(guān)注和報道��。
BGM0504是采用分子動(dòng)力學(xué)模擬技術(shù)(Molecular Dynamics, MD)輔助設計的GLP-1和GIP雙受體激動(dòng)劑���,在體外和體內實(shí)驗中均顯示出卓越的療效����。
研究團隊利用分子動(dòng)力學(xué)模擬技術(shù)���,發(fā)現了GLP-1R和GIPR上的特定氨基酸殘基與備選多肽激動(dòng)劑相應位置的氨基酸側鏈之間可能出現穩定的鹽橋作用��。該鹽橋作用不僅可以進(jìn)一步穩定備選多肽激動(dòng)劑與雙受體的結合穩定性���,更有利于穩定雙受體的激活態(tài)構象��。而這種相互作用并未被先前的晶體學(xué)研究或冷凍電鏡研究所確認發(fā)現�����。
隨后��,BGM0504的設計將?�;稽c(diǎn)移至第40位氨基酸位點(diǎn)�。通過(guò)這種設計���,將多肽分子對GLP-1R和GIPR的激動(dòng)作用相較于替爾泊肽提升到三倍���,同時(shí)保持了良好的藥物體內半衰期����,在糖尿病和肥胖癥小鼠模型中均取得了卓越的治療效果�����。
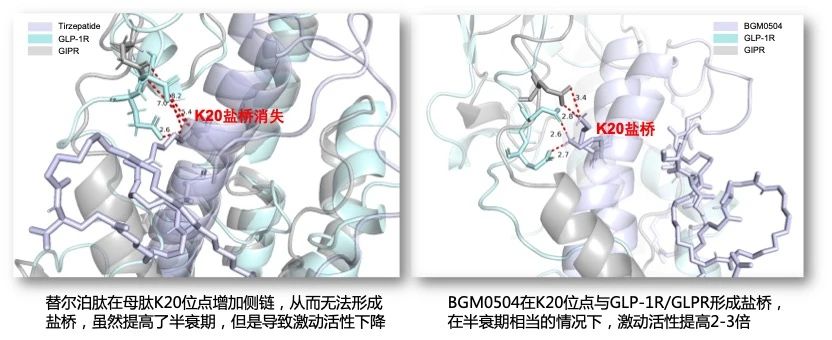
圖1. K20鹽橋:BGM0504比替爾泊肽強2-3倍激動(dòng)活性的關(guān)鍵
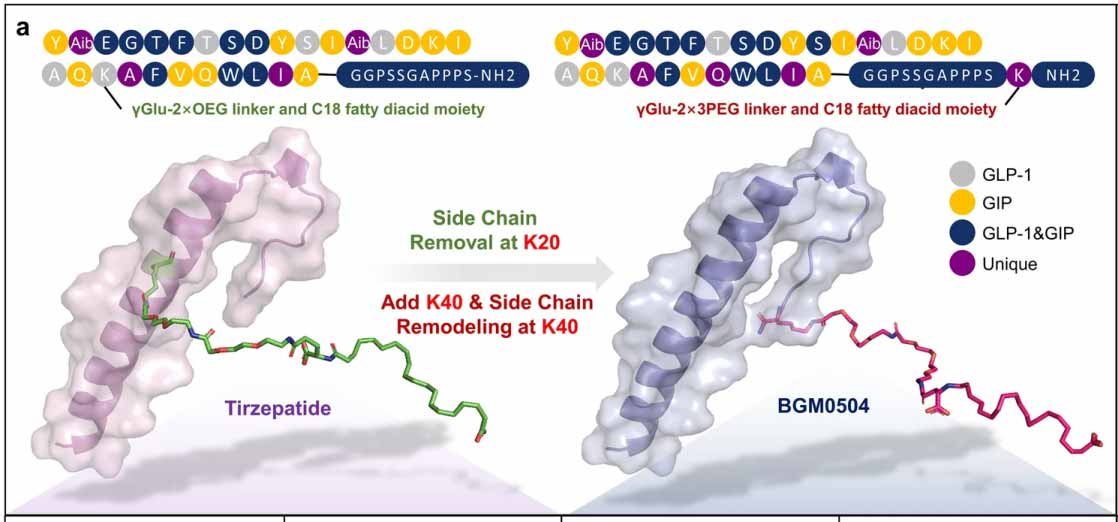
圖2. BGM0504理性設計后的結構對比(來(lái)自Nature子刊文章)
在體內外實(shí)驗的研究中��,BGM0504相比Tirzepatide在GLP-1R/GIPR上提升到3倍的激動(dòng)活性�����,這解釋了BGM0504在小鼠體內的研究中能夠具有更加好的降糖和減重的效果的原因�����。此外�����,BGM0504相比Tirzepatide與人血清白蛋白具有更強的結合能力��。在關(guān)鍵的大鼠和食蟹猴的藥代動(dòng)力學(xué)研究中�,實(shí)驗動(dòng)物在BGM0504不同的劑量下表現出很好的耐受性�,且BGM0504的半衰期能夠達到一周注射一次的效果���,同時(shí)具有持續較高的血藥暴露量來(lái)維持藥效的發(fā)揮����。這些研究表明�����,BGM0504作為一種用于治療糖尿病和肥胖癥的多肽藥物具有良好的安全性和有效性��。
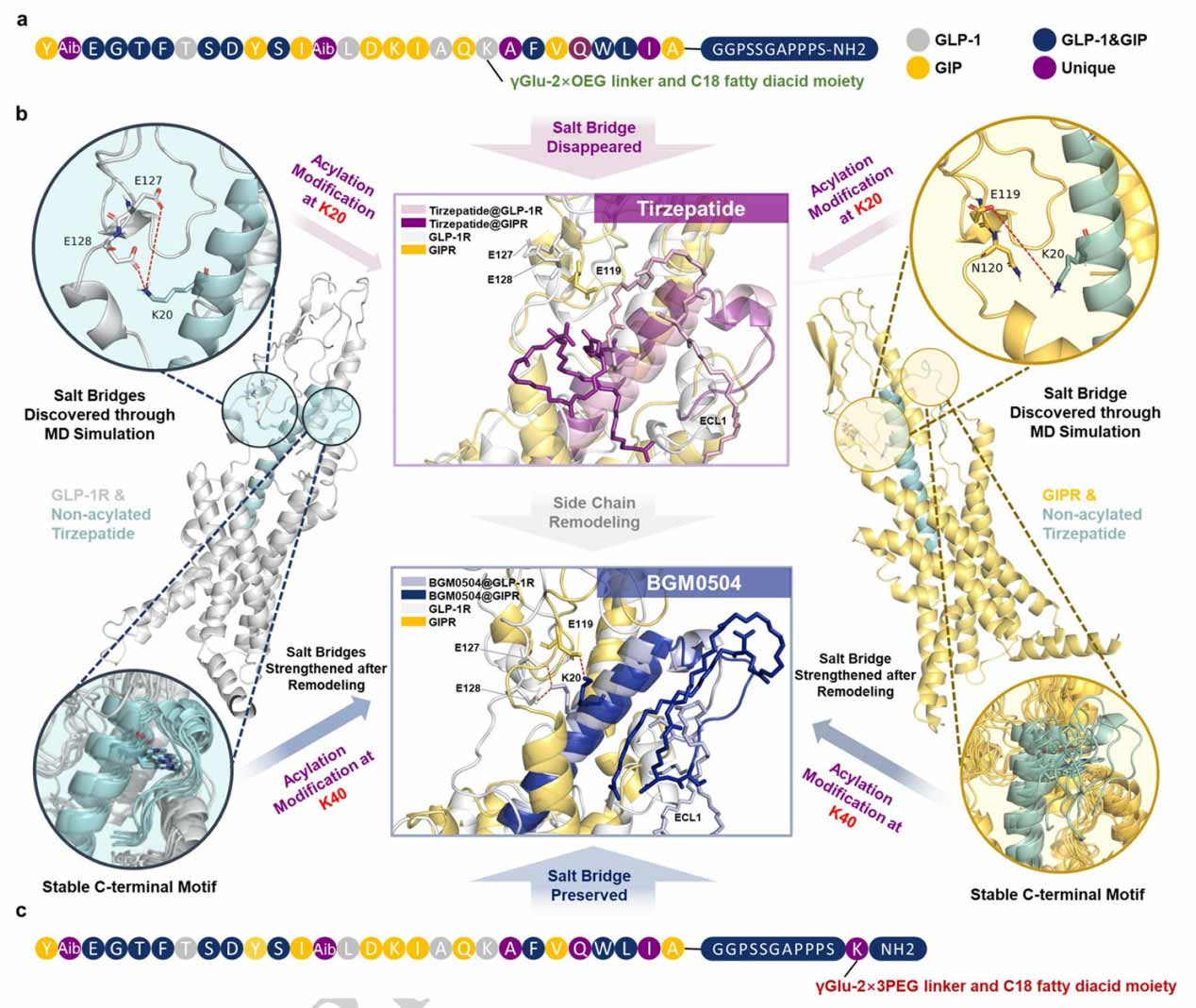
圖3. 替爾泊肽和BGM0504的結構分析對比和優(yōu)化策略(來(lái)自Nature子刊文章)
在此基礎上��,予路乾行正在與博瑞醫藥開(kāi)展全方位合作�,利用分子動(dòng)力學(xué)模擬平臺結合AI技術(shù)����,助力多條新藥研發(fā)管線(xiàn)的快速推進(jìn)���。
博瑞醫藥(股票代碼:688166.SH)是一家專(zhuān)注于開(kāi)發(fā)高端藥品的創(chuàng )新型制藥公司��。公司整合了原料藥和制劑�,結合仿制藥和創(chuàng )新藥���,以滿(mǎn)足全球臨床需求�����。BGM0504 注射液是博瑞醫藥(688166.SH)自主研發(fā)的 GLP-1和 GIP受體雙重激動(dòng)劑���,可激動(dòng)GIP和 GLP-1下游通路����,產(chǎn)生控制血糖�、減重和治療非酒精性脂肪性肝炎(NASH)等生物學(xué)效應��,展現多種代謝疾病治療潛力�����。
予路乾行是一家以人工智能���、量子力學(xué)及分子模擬算法為核心技術(shù)�����,通過(guò)模擬運算賦能新藥研發(fā)的交叉學(xué)科技術(shù)驅動(dòng)型生物醫藥公司�����。公司結合多尺度分子動(dòng)力學(xué)模擬技術(shù)和AI算法�,通過(guò)打造獨創(chuàng )的“分子電影”數據及算法平臺��,揭示復雜生物體系的動(dòng)態(tài)分子機制��,填補了針對難成藥靶點(diǎn)藥物研發(fā)領(lǐng)域的空白����。公司提供各類(lèi)計算化學(xué)服務(wù)����,合作方式靈活����,可在PCC之前的各個(gè)階段提供幫助�。適用的模式包括小分子���、PROTAC�����、ADC����、抗體�、多肽�、融合肽��、XDC等��。
參考資料
[1] Yuan, J., Liu, W., Jiang, X. et al. Molecular dynamics-guided optimization of BGM0504 enhances dual-target agonism for combating diabetes and obesity. Sci Rep 14, 16680 (2024). https://doi.org/10.1038/s41598-024-66998-8
[2] https://www.prnewswire.com/news-releases/nature-study-reveals-ai-and-molecular-dynamics-designed-bgm0504-exhibits-superior-potency-302202619.html
[3] https://apnews.com/press-release/pr-newswire/clinical-trials-medication-artificial-intelligence-e9f0ac1f75948e0bb0acf98a3b62cdea
[4] https://www.asahi.com/and/pressrelease/424914237/?