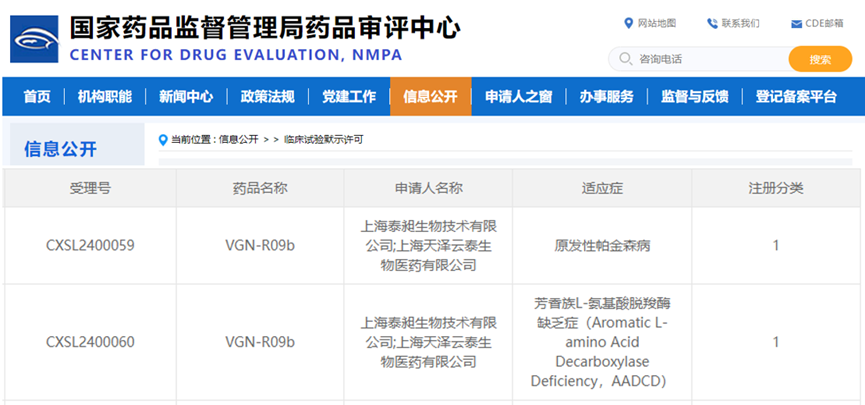
近日����,上海天澤云泰生物醫藥有限公司及其全資子公司上海泰昶生物技術(shù)有限公司(以下簡(jiǎn)稱(chēng)“公司”)自主研發(fā)和生產(chǎn)的VGN-R09b獲得國家藥品監督管理局(以下簡(jiǎn)稱(chēng)“國家藥監局”)簽發(fā)的藥物臨床試驗批準通知書(shū)��,同意開(kāi)展治療原發(fā)性帕金森?���。≒D)和芳香族L-氨基酸脫羧酶缺乏癥(AADCD)的臨床試驗�����。
VGN-R09b是國內首個(gè)采用AAV遞送雙基因策略獲批注冊臨床的基因療法�,也是首個(gè)從治療罕見(jiàn)病拓展到常見(jiàn)病的獲批注冊臨床的基因治療藥物�,是該產(chǎn)品及公司發(fā)展的一個(gè)重要里程碑��。
公司董事長(cháng)趙小平博士表示:本次國家藥監局批準VGN-R09b同時(shí)開(kāi)展兩個(gè)適應癥的臨床試驗����,是從監管和科學(xué)的角度對VGN-R09b在目標人群使用安全���、潛在獲益以及產(chǎn)品質(zhì)量的肯定�����,希望VGN-R09b以它良好的安全性和優(yōu)越的有效性造福更多的患者��。
帕金森?��。≒D)是第二常見(jiàn)的神經(jīng)退行性疾病���,且帕金森病患病率的增長(cháng)比許多其他神經(jīng)退行性疾病更快�����。帕金森病估計影響到約1%的65歲以上人口和4%的85歲以上人口����。中國65歲以上人群患病率為1.7%�,與歐美國家相似��。未來(lái)我國帕金森病患病人數將從2005年的199萬(wàn)人上升到2030年的500萬(wàn)人���,幾乎占全球帕金森病患病人數的一半���。
AADC(芳香族L-氨基酸脫羧酶)缺乏癥是由于編碼AADC的DDC基因中存在致病性突變��,而AADC負責使L-DOPA(左旋多巴)和5-HTP(5-羥基色氨酸)分別形成神經(jīng)遞質(zhì)多巴胺和5-羥色胺的脫羧酶��。AADC的缺失影響了控制交感神經(jīng)系統��、情緒��、認知和運動(dòng)協(xié)調的關(guān)鍵神經(jīng)遞質(zhì)的合成��,表現為運動(dòng)功能障礙���、智力障礙和警覺(jué)性減弱及睡眠障礙等臨床癥狀����,在生命的前十年內有過(guò)早死亡的危險����。目前�,該疾病中國還沒(méi)有正式的流行病學(xué)研究��,在臺灣開(kāi)展的一項新生兒AADC缺乏癥篩查項目�,發(fā)現AADC缺乏癥的出生發(fā)病率約為1/ 32,000�。
VGN-R09b是公司自主研發(fā)和生產(chǎn)的基因治療產(chǎn)品����,使用重組AAV作為基因治療載體��,以遞送有功能的AADC為基礎恢復多巴胺的生成��,從而發(fā)揮相應的潛在的治療作用�����。通過(guò)局部紋狀體注射的方式����,使藥物能夠直接作用于發(fā)病部位�����,減少全身的給藥劑量�����,從而減少相應的免疫反應等不良反應�。理論上�,基因治療只需要注射一次就能起到相應的長(cháng)期療效�����。
天澤云泰2020年3月注冊成立于中國上海���,致力于將前沿的基因及細胞治療技術(shù)�����,轉化為臨床可及的治療方法��,以期造福更多患者���。
天澤云泰擁有具有自主知識產(chǎn)權的ViVec?AAV載體篩選平臺�、ViLNP?脂質(zhì)納米粒技術(shù)平臺����、ViCas?CRISPR基因編輯技術(shù)平臺和ViHiYi?AAV高產(chǎn)技術(shù)平臺����,通過(guò)基因替代�、基因調控和基因編輯等策略���,開(kāi)發(fā)治療中樞神經(jīng)系統疾病����、代謝及血液系統疾病����、眼科疾病等領(lǐng)域的創(chuàng )新基因治療藥物���,擁有包括多個(gè)潛在First-in-class產(chǎn)品的多元化管線(xiàn)�����。
目前�����,天澤云泰已經(jīng)獲得多家知名基金的多輪投資��,分別在張江高科技園區���、北京巢生實(shí)驗室����、臨港新片區和外高橋自貿區建成面積2,500平米的基因治療研發(fā)運營(yíng)中心�、基因編輯技術(shù)研發(fā)中心���、3,000平米的基因治療中試生產(chǎn)車(chē)間和5,500平方米GMP商業(yè)化生產(chǎn)車(chē)間�。