
作為一家世界排名前十以創(chuàng )新為驅動(dòng)的全球性生物制藥企業(yè)�����,阿斯利康站在世界生命科技的最前沿��,每年在新藥研發(fā)上投入高達40億美元以上����。這項題為 “Development and validation ofblood tumor mutational burden reference standards” 的研究報告展示了bTMB對照標準的開(kāi)發(fā)和驗證數據�,其中使用了慧渡醫療600基因的PredicineATLAS?評估突變覆蓋率���、突變等位基因頻率和bTMB評分��。該報告的bTMB對照標準可支持bTMB平臺的校準和驗證�����,統一bTMB評分標準��,從而提高檢測的準確性�����,幫助臨床醫生進(jìn)行腫瘤治療方案決策�����。

TMB(Tumor Mutation Burden���,腫瘤突變負荷)��,是指腫瘤基因組中平均1Mb范圍內所包含的體細胞蛋白編碼區點(diǎn)突變����、插入缺失等基因變異數量��?����;谀[瘤組織樣本計算的TMB為腫瘤TMB(tTMB)���,基于血液樣本計算的TMB為血液TMB(bTMB)���。TMB作為免疫治療的生物標志物����,用于評估接受免疫靶向治療的患者是否能夠獲益����。
目前����,由于實(shí)驗方法�����、基因數量以及生物信息學(xué)分析等方面的差異��,行業(yè)內缺乏統一的bTMB計算和評估標準�����。Friends of Cancer Research (FoCR) TMB Harmonization Consortium提出了對tTMB分析的評估對照標準����,實(shí)現不同NGS計算標準化����,確定Panel-TMB評分和WES-TMB評分之間的相關(guān)性��。bTMB分析具有獨特的挑戰�����,需要更高的靈敏度�����,因此建立bTMB的參考標準更加重要�����。
該研究采用腫瘤細胞系和供體匹配的淋巴母細胞系的DNA制作的人工bTMB作為對照��,校準和比對不同實(shí)驗室�����、不同Panel bTMB平臺評分結果�����。
研究發(fā)現����,慧渡醫療的PredicineATLAS?和Guardant Health的GuardantOMNI兩個(gè)平臺���,bTMB評分分別為7��、20和26 mut/Mb�����,與對照標準品一致��,表現出良好的可重復性����。這項研究表明了在一系列bTMB水平上制定bTMB參考標準的可行性�。
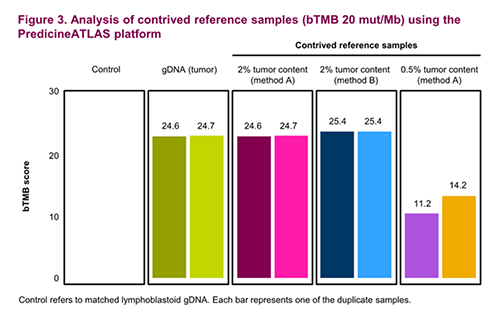
慧渡醫療bTMB評分結果與對照標準品結果一致
為研究血液中bTMB對PDL1/CTLA4聯(lián)合免疫治療效果評估����,阿斯利康采用慧渡醫療600基因PredicineATLAS? ctDNA液態(tài)活檢NGS技術(shù)平臺����,對174例mPDAC患者進(jìn)行血液ctDNA 的腫瘤相關(guān)基因檢測����,涵蓋腫瘤藥物開(kāi)發(fā)管線(xiàn)中從靶向治療到免疫治療的相關(guān)基因����,包括點(diǎn)突變��、融合�����、插入缺失�、擴增��、大片段缺失和血液TMB��,MSI等�����,從分子水平預測和評估mPDAC患者對于免疫治療藥物的敏感性�����。該研究的bTMB等生物標記物結果將在2021年1月的ASCO-GI國際會(huì )議上專(zhuān)題報道��。
與阿斯利康的三度合作���,再次體現了慧渡醫療 “起點(diǎn)就是業(yè)界頂點(diǎn)” 的從業(yè)標準和打造精品的堅定決心����。選擇從歐美藥企出發(fā)�,慧渡醫療開(kāi)發(fā)出國際領(lǐng)先的新一代液態(tài)活檢技術(shù)����、精準臨床試驗的全球解決方案和在中美同步運營(yíng)的CAP和CLIA實(shí)驗室網(wǎng)絡(luò )�����,與世界排名前十的歐美藥企和國內外頂級專(zhuān)家和醫療機構深度合作���,通過(guò)基于血液��、尿液和組織的一站式生物標記物平臺體系來(lái)支持全球新藥臨床試驗��、伴隨診斷開(kāi)發(fā)和癌癥早篩�。
查看SITC2020英文報告原文�,請點(diǎn)擊“閱讀原文”鏈接:
關(guān)于慧渡
慧渡醫療?是一家專(zhuān)注于精準醫療的高科技集團公司�����。堅持??“起點(diǎn)就是業(yè)界頂點(diǎn)” 的從業(yè)標準����,打造液態(tài)活檢行業(yè)精品���。
從歐美藥企出發(fā)�����,慧渡醫療業(yè)界獨創(chuàng )ctRNA + ctDNA 聯(lián)合液態(tài)活檢技術(shù)���、精準臨床試驗的全球解決方案和在中美同步運營(yíng)的CAP和CLIA實(shí)驗室網(wǎng)絡(luò )��,與世界排名前十的歐美藥企和國內外頂級專(zhuān)家和醫療機構深度合作���,通過(guò)基于血液��、尿液和組織的一站式生物標記物平臺體系來(lái)支持全球新藥臨床試驗��、伴隨診斷開(kāi)發(fā)和癌癥早篩�����。