在剛剛落下帷幕的ASCO20國際臨床腫瘤學(xué)研究盛會(huì )上��,阿斯利康正式發(fā)布了與慧渡醫療合作的ctDNA液態(tài)活檢助力膽管癌臨床試驗的積極臨床數據����。這是世界上首例 D+T (杜魯伐單抗Durvalumab + 曲美單抗Tremelimumab) 聯(lián)合免疫治療的國際二期臨床試驗���。該報告的發(fā)布旋即引起業(yè)界高度關(guān)注�����,成為各大藥企和臨床醫學(xué)專(zhuān)家關(guān)注討論的熱點(diǎn)話(huà)題��。
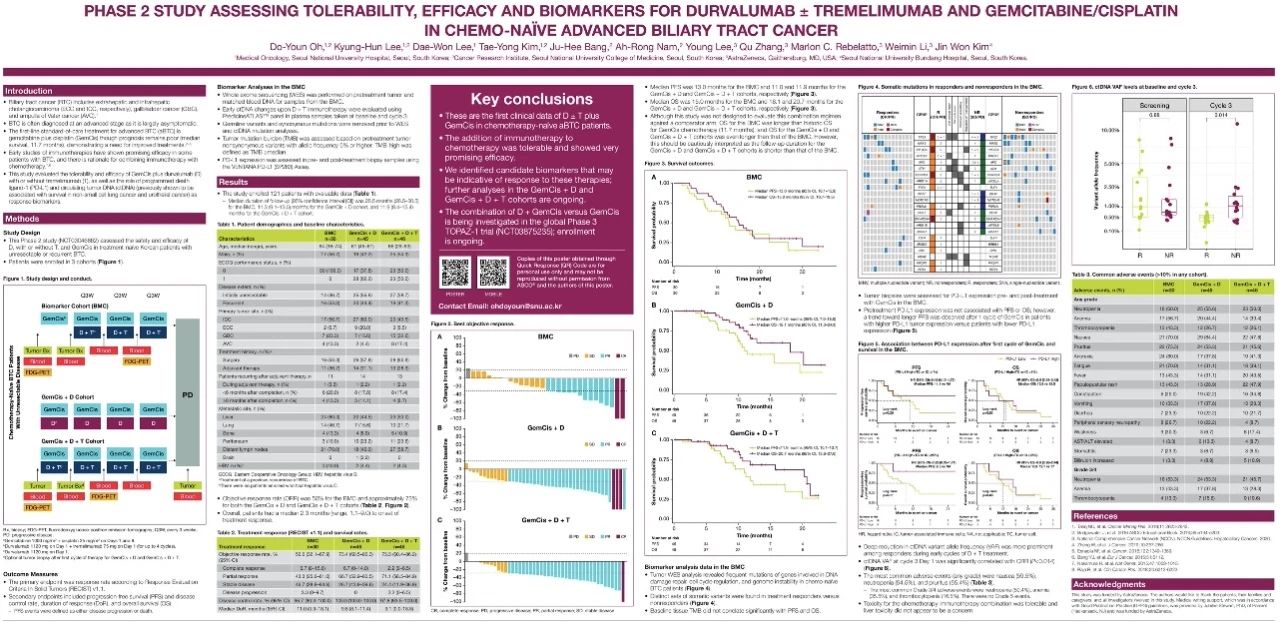
研究回顧
該研究采用目前歐美國際上最全面的慧渡醫療600基因PredicineATLAS? ctDNA液態(tài)活檢NGS技術(shù)平臺���,對121例未經(jīng)化療的晚期膽管癌患者 (advanced Biliary Tract Cancer, aBTC) 進(jìn)行血液ctDNA的腫瘤相關(guān)基因生物標志物檢測���,涵蓋腫瘤藥物開(kāi)發(fā)管線(xiàn)中從靶向治療到免疫治療的相關(guān)基因����,包括基因點(diǎn)突變����、融合���、插入缺失��、擴增��、大片段缺失和血液TMB等���。
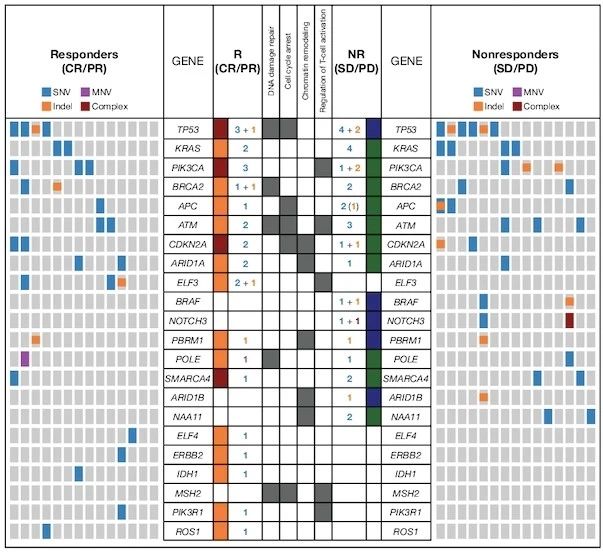
Somatic mutations in responders and non-respondersin the BMC
液態(tài)活檢結果顯示�����,患者血液中ctDNA基因變異 (VAF) 的動(dòng)態(tài)變化幅度在對聯(lián)合免疫治療療效敏感的患者中更為明顯��。尤其在第3個(gè)療程時(shí)�����,患者血液中的ctDNA基因變異 (VAF) 程度與對藥物治療的總體應答率 (ORR) 具有顯著(zhù)的統計學(xué)相關(guān)性 (p<0.014)�����。相反��,基于腫瘤組織的腫瘤突變負荷 (TMB) 與無(wú)進(jìn)展生存期 (PFS) 和總生存期 (OS) 無(wú)關(guān)���。
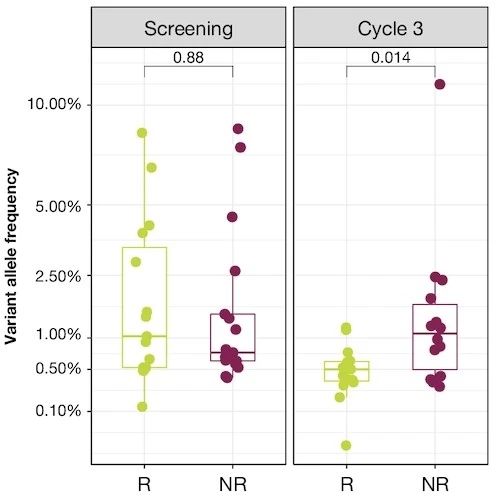
ctDNA VAF levels at baseline and C3D1
液態(tài)活檢���,技術(shù)當先
液態(tài)活檢猶如大海撈針����,在體液中篩選十億分之一的癌癥特異性突變是對技術(shù)的嚴肅考驗�。
本著(zhù)“起點(diǎn)就是業(yè)界頂點(diǎn)”的從業(yè)原則���,慧渡醫療經(jīng)歷近五年的臥薪嘗膽開(kāi)發(fā)出新一代“基因雷達”技術(shù)��,完美解決目前對液態(tài)活檢行業(yè)挑戰難度最大的ctDNA大片段基因缺失(比如BRCA, PTEN��,RB等)和ctRNA剪切體變異�����。針對血液TMB和常規的基因變異(點(diǎn)突變�、融合���、插入缺失��、擴增)����,慧渡醫療ctDNA液態(tài)活檢技術(shù)媲美國際先驅企業(yè)Guardant Health����。相關(guān)技術(shù)評估歷經(jīng)歐美學(xué)術(shù)界和藥企的對比驗證����,相關(guān)文章近期在European Urology, Breast Cancer Research, EBioMedicine等國際學(xué)術(shù)期刊上相繼發(fā)表��。
臨床試驗�、強強聯(lián)合
液態(tài)活檢檢測結果的準確性和特異性可以左右腫瘤患者的臨床治療方案選擇��,關(guān)系到26億美元平均成本的腫瘤新藥臨床試驗的成敗與否�。
做為當今腫瘤新藥開(kāi)發(fā)的國際領(lǐng)軍企業(yè)�,阿斯利康選擇與慧渡醫療在歐美和中國進(jìn)行全球新藥臨床試驗合作����,代表了國際頂尖藥企對慧渡醫療創(chuàng )新技術(shù)的客戶(hù)認可和全球運營(yíng)的行業(yè)背書(shū)�。
繼今年年初與德國Merck合作在A(yíng)ACR液態(tài)活檢峰會(huì )上聯(lián)合報告液態(tài)活檢的科研合作�,慧渡醫療與更多國際藥企的全球臨床試驗合作結果將在下半年的ESMO會(huì )議上陸續報道�����。
立足中國��、放眼全球
為提高新藥臨床試驗的成功率和實(shí)現基于生物標記物的中美臨床試驗一體化��,慧渡醫療推出“精準臨床試驗的全球解決方案”和其在中美同步運營(yíng)的CAP和CLIA實(shí)驗室網(wǎng)絡(luò )���,為國際和國內藥企提供基于血液�����、尿液和組織的“一站式”生物標記物檢測服務(wù)平臺和伴隨診斷臨床報批來(lái)支持在中國和歐美進(jìn)行的全球新藥臨床試驗�。
目前��,慧渡醫療與國內外藥企及頂尖醫療機構和醫學(xué)專(zhuān)家建立了密切合作�����,通過(guò)對癌癥相關(guān)基因生物標記物的精準檢測和Umbrella + Basket復合臨床試驗設計���,實(shí)現患者的篩查和精準入組臨床試驗�,縮短臨床入組時(shí)間��,精準治療腫瘤患者����,從而提高臨床試驗成功率�����。
查看2020ASCO英文報告更多內容�,請點(diǎn)擊以下鏈接:
2020 ASCO膽管癌研究報告
Phase II study assessingtolerability, efficacy, and biomarkers for durvalumab ± tremelimumab andgemcitabine/cisplatin in chemo-na?ve advanced biliary tract cancer?
關(guān)于慧渡醫療
慧渡醫療是一家專(zhuān)注于精準醫療的高科技集團公司���。我們致力于研究腫瘤分子機制�����,開(kāi)發(fā)用于癌癥診斷和用藥監測的基因檢測方法及生物信息學(xué)算法��,通過(guò)我們的技術(shù)來(lái)推動(dòng)腫瘤診斷和治療的發(fā)展�����。
精英團隊:慧渡醫療核心團隊成員來(lái)自于全球頂尖的工業(yè)界和學(xué)術(shù)界��,開(kāi)發(fā)出第二代基于RNA和DNA聯(lián)合檢測的液態(tài)活檢技術(shù)�,應用于新藥臨床試驗�、癌癥早篩和臨床用藥指導�����。
業(yè)界國際背書(shū):目前�����,慧渡醫療已經(jīng)與30多家國際知名藥企(包括8家世界500強企業(yè))��、世界各地的頂尖醫療機構�����、大學(xué)����、政府和全球健康產(chǎn)業(yè)的相關(guān)機構開(kāi)展了全方位的戰略和業(yè)務(wù)合作��?��;鄱舍t療的液態(tài)活檢技術(shù)被應用于多項基于生物標記物的臨床二期和三期全球精準新藥臨床試驗��,得到歐美國際藥企和國內外醫學(xué)專(zhuān)家的高度認可和臨床采用�����,為建立全球智慧醫學(xué)數據庫積累了寶貴的數據���。
獨創(chuàng )技術(shù)和核心實(shí)力:慧渡醫療業(yè)界獨創(chuàng )ctRNA+ctDNA聯(lián)合液態(tài)活檢解決方案�����,在基因組學(xué)和轉錄組學(xué)層面上發(fā)現腫瘤相關(guān)的基因突變���,具備無(wú)創(chuàng )傷�����、高敏感���、克服異質(zhì)性的特性��,成功實(shí)現對癌癥患者的精準診斷�、靶向用藥指導�����、療效動(dòng)態(tài)監控和抗藥性分子機制的分析�����。為加速新藥臨床試驗�,慧渡醫療推出了“精準臨床試驗的全球解決方案”����,通過(guò)與Predicine合作建設的在美國硅谷�、中國上海的CLIA和CAP國際標準實(shí)驗室�,提供一站式���、全方位的生物標記物檢測����、生物信息學(xué)和數據解讀的綜合平臺��,支持在中國-美國-歐洲-亞洲-澳洲同步進(jìn)行的國際多中心新藥臨床試驗�。

業(yè)務(wù)合作����,請聯(lián)系:info@huidumed.com