全世界約有2.37億人患有癥狀和活動(dòng)限制性骨關(guān)節炎(OA)����,這是全球范圍內與殘疾有關(guān)的第三大疾病����。在疾病的最后階段�����,通常需要進(jìn)行全膝置換����。OA可能是美國全髖關(guān)節和膝關(guān)節置換的首要原因��。我國OA患者超過(guò)1億�,在60歲以上人群患病率為50%����,而在75歲以上人群則高達80%�����。該病致殘率高��,嚴重影響生活質(zhì)量���,給患者和社會(huì )帶來(lái)極大的痛苦和沉重的負擔��。目前尚無(wú)有效治療藥物可以用于治療OA�,主要還是以緩解疼痛�、阻止和延緩疾病的進(jìn)展為目的���。但這并不能從根本上改善關(guān)節軟骨的病變��。藥物治療無(wú)效的重度骨關(guān)節炎患者�,將會(huì )考慮實(shí)施關(guān)節置換手術(shù)��。顯然����,安全的�、可以促進(jìn)受損關(guān)節軟骨再生的治療方式��,將解決一個(gè)關(guān)鍵的未滿(mǎn)足的醫療需求���。
目前FDA和NMPA還沒(méi)有批準用于預防或減緩OA進(jìn)展的藥物�����,LH021將是國內NMPA批準進(jìn)入臨床的首個(gè)疾病改善型藥物(DMOAD藥物)����。
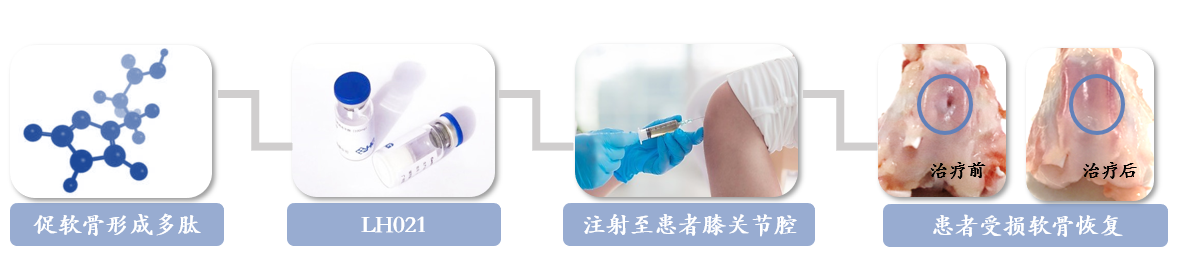
LH021是合成的多肽新藥�����,氨基酸序列源自BMP等促骨形成蛋白�����,它可以誘導軟骨細胞增殖和促進(jìn)細胞外基質(zhì)(ECM)生成��,臨床前模型表明其具有促進(jìn)軟骨生長(cháng)和修復的潛力��。該新藥2019年5月獲得CDE的化學(xué)1類(lèi)新藥的默許臨床并同意批準使用膝關(guān)節炎病人進(jìn)行I期臨床研究���。2019年年底領(lǐng)晟與廣東省中醫院臨床機構開(kāi)始啟動(dòng)臨床招募�����。領(lǐng)晟已對LH021進(jìn)行了全球專(zhuān)利保護��,其中國�����、美國和歐洲專(zhuān)利都已授權��,并計劃將在完成國內I期研究后啟動(dòng)美國的IND申報�。
領(lǐng)晟計劃2020年完成首個(gè)I期���,除研究用藥安全性外��,會(huì )延長(cháng)隨訪(fǎng)觀(guān)察���,進(jìn)一步探索藥物軟骨修復作用及疼痛改善等指標�����。這部分數據將在2021年的美國AAOS和歐洲骨科年會(huì )年會(huì )上公布����。
領(lǐng)晟CEO宋燕博士說(shuō):“LH021項目臨床首次成功給藥令我們深受鼓舞��,LH021作為國內首個(gè)DMOAD藥物��,有望給千萬(wàn)深受骨關(guān)節疾病折磨的患者帶來(lái)新的根本性的治療方法����,我們相信使用LH021后有助于患者的軟骨修復���,平滑��,厚度增加�����,不僅可能減少疼痛也有望提高患者的行動(dòng)能力和生活質(zhì)量�。我們致力于給這些尚未滿(mǎn)足的臨床需求帶來(lái)新的療法����?�!?/span>
讓我們共同期待骨關(guān)節炎新藥盡快進(jìn)入市場(chǎng)���,造?�;颊?����。
關(guān)于骨修復治療領(lǐng)域
骨修復是廣州領(lǐng)晟致力于重點(diǎn)開(kāi)發(fā)的治療領(lǐng)域����,主要包括軟骨修復和硬骨修復����,包括骨關(guān)節炎����,軟骨損傷�����,骨不連���,股骨頭壞死等多個(gè)缺乏治療手段的未滿(mǎn)足臨床需求���。骨修復板塊包括1類(lèi)新藥LH021�,活性骨材料Carti-Gel以及其Combination產(chǎn)品����。首個(gè)產(chǎn)品有望2021年申報上市�。
關(guān)于臨床研究機構及計劃
本項目由廣東省中醫院曾星教授和林定坤教授以及中山大學(xué)附屬第一醫院傅明教授和董吁鋼教授牽頭���,計劃入組38例符合入排的原發(fā)性膝骨關(guān)節炎患者����,通過(guò)單次和多次劑量遞增研究考察LH021的耐受性��、安全性和藥代特點(diǎn)�,同時(shí)探索LH021的劑量跟療效以及軟骨合成和代謝相關(guān)生物標記物的關(guān)系��,為II期臨床試驗給藥方案的制定提供依據����。
關(guān)于領(lǐng)晟醫療
廣州領(lǐng)晟醫療科技有限公司專(zhuān)注于解決全球未被滿(mǎn)足的醫療需求���,并力爭為中國及亞太地區的患者提供可負擔的消化科��、骨科等慢性疾病的解決方案�����。通過(guò)自主研發(fā)以及全球技術(shù)引進(jìn)�����,領(lǐng)晟儲備了12個(gè)不同階段的創(chuàng )新藥物品種�,覆蓋腫瘤放化療藥物���、功能性消化疾病等重大的慢性疾病領(lǐng)域以及老齡化相關(guān)的骨科疾病�����,其中1項NDA���,8項臨床階段新藥/械品種����,首個(gè)產(chǎn)品有望在2021年啟動(dòng)銷(xiāo)售�。